日期:2022-06-30 22:57:32 来源:中华检验医学网 点击: 次
作者 | 万权松 章芊秋
指导老师 | 刁杨丽
单位 | 隆昌市人民医院医学检验科
依据新冠诊疗第九版,新型冠状病毒核酸检测阳性为确诊新冠感染的首要标准,从事新冠病毒核酸检测的实验室应严格做好室内质控,以确保新冠核酸检测结果准确可靠,那么新冠核酸检测的室内质控应当怎么做呢?
医疗机构新型冠状病毒核酸检测工作手册(以下简称“手册”)中“五、实验室质控控制与管理”的室内质控要求:实验室应按照《国家卫生健康委办公厅关于医疗机构开展新型冠状病毒核酸检测有关要求的通知》(国卫办医函〔2020〕53号)要求规范开展室内质控。每批检测至少有1份弱阳性质控品(第三方质控品,通常为检出限的1.5-3倍)、3份阴性质控品(生理盐水)。质控品随机放在临床标本中,参与从提取到扩增的全过程[1]。
作为核酸检测人员,在实际操作中应当怎么去实施这一要求呢?采用阴性、弱阳性质控的目的又是什么呢?
手册要求每批检测需要至少加入3份阴性质控和1份弱阳性质控,新冠核酸室内质控的目的是最大可能的检出检测中的随机误差和系统误差,因此在整个核酸提取实验的过程中,上述阴、阳性质控标本应当均匀分布在患者标本中间,以充分反应实际检测中可能存在的问题。
关于质控品的具体放置位置,应注意的是所谓均匀分布于标本中间,不应当一层不变,固定于某些孔位,应当对所有的孔位起到监测的效果,在一定的时间内,尽可能保证每个孔都进行过质控的监测,从而更好的保证每个孔的扩增有效性[2]。
与生化、免疫等室内质控不同的是,PCR核酸检测需要设置阴性质控,其目的为:1.监测实验室扩增产物残留的“污染”;2.由当次实验过程中引起的污染,如阳性质控使用未瞬离,开盖不慎气溶胶经过程污染实验;3.试剂污染。
对于3份阴性质控标本,可采用1份试剂盒自带阴性对照、1份生理盐水、1份过往阴性标本作对照,更好的监测污染的发生,避免假阳性。阴性质控若检测出阳性,说明上述实验过程某环节出现问题,应当停止实验检测,立即查找原因,避免更大污染的发生。阳性质控品可采用1份第三方弱阳性质控和1份试剂盒自带阳性对照,可以更好的监测假阴性的发生。
在定性测定中,如果使用高浓度的样本,测定操作的变化不是特别大的情况下,对定性测定结果的影响不会那么明显,弱阳性质控标本能更敏感的监测假阴性的发生。因此通常使用的弱阳性样本为检出限的1.5-3倍[3]。
对于质控结果的判断:弱阳性质控品检测为阳性,阴性质控品检测为阴性,若采用内源性内标参与提取扩增,则生理盐水内标不出,阴性标本内标正常,试剂厂家自带阴性质控品根据试剂说明判断内标情况,视为在控,则报告可以发出;反之,则为失控,不可报告,应分析失控原因,必要时重新检测。
新冠核酸检测阳性质控标本测定结果可与生化、免疫、血常规等采用传统的Levey-Jennings(L-J)质控图记录表示,横坐标X轴表示代表检测时间或测定的批次,纵坐标Y轴表示检测结果,根据阳性质控品的均值和标准差的倍数绘制质控图。
乙肝病毒(HBV-DNA)是PCR实验室比较熟悉的项目,临床医生通过对病毒载量的定量监测来评估患者治疗的效果,为了保证实验室检测结果的可靠性,更好的了解实验室的精密度,通常会将病毒载量结果通过对数转换,参照最大允许总误差0.4log,绘制L-J质控图[2]。
而目前新冠核酸检测,实验室为定性检测结果,目前未找到对应最大允许总误差(TEa)的相关依据,PCR核酸检测中的CT值可在一定程度下反应病毒载量的多少,因此可采用已知浓度的质控品CT值的变化反映不同批次中检测结果的一致性,从而反映检测结果的可靠性,例如本科室采用的第三方浓度已知的质控品,新冠核酸检测N基因、ORF基因CT值均为35左右。将每批次检测结果保存原始数据,质控品的CT值记录于lis中,再绘制成质控图,举例如下:
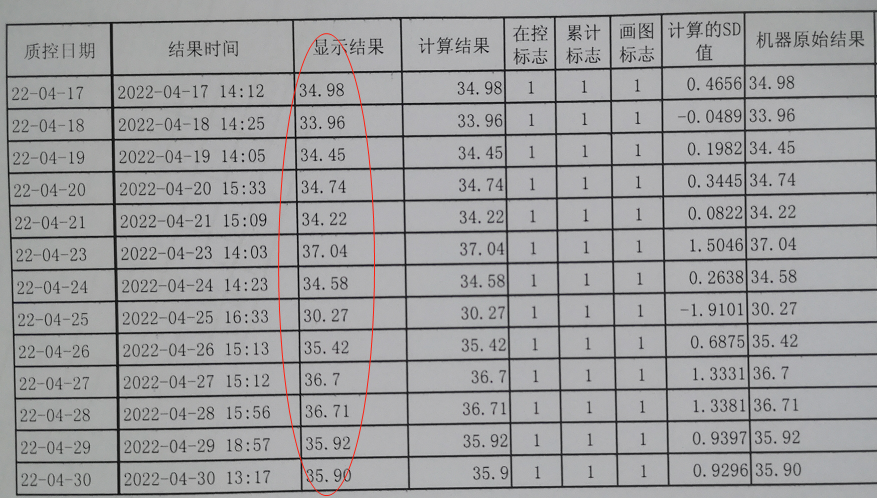
图1 我科使用第三方质控品检测新冠病毒核酸ORF基因的CT值
绘制质控图如下:
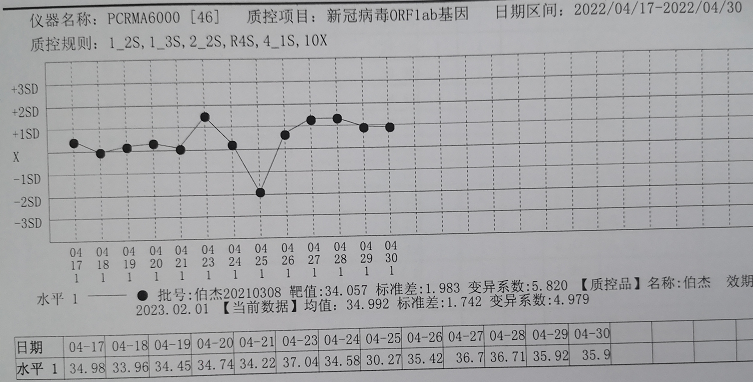
图2 新冠病毒核酸ORF基因的CT值汇总后绘制的质控图
图1、图2仅为新冠核酸检测针对ORF基因设计的质控图,目前国内获批的新冠病毒核酸检测试剂盒多针对多个基因,实验室可同时分析针对不同基因的室内质控数据建立对应的质控图。
注:新冠核酸检测报告为定性报告,CV的设置可参考试剂说明书中精密度要求设置,失控规则可参照Westgard多规则。
第三方质控涵盖新冠病毒核酸的RdRp、E、N、ORF1a、ORF1b和S基因,不单独针对新冠核酸检测试剂厂商的基因位点,因此使用时需严格按照SOP进行,避免导致实验室污染。若为液体质控,混匀瞬离后与标本同样方式加入检测即可;若为干粉质控,需瞬离后方可轻拧瓶盖,加入去离子水混匀,混匀后瞬离作为待测标本使用,瞬离可使质控品下沉,避免开盖时引发气溶胶污染。
可将试剂直接扩增,若出现阳性,则考虑试剂污染,更换试剂可解决。
考虑扩增产物污染时,可将3-5只空采样管开盖放置实验室内半小时后检测,若出现阳性,则应立即停止实验室新冠核酸检测,全面清洁实验室,待污染消除后再行检测。
大多数来自于阳性质控标本,可能由于操作不规范导致质控溢出引起等随机误差引起,可用生理盐水代替临床样本模拟检测,以排除可能存在的实验室污染。
操作不当……
大多为质控品引起,首先检查质控品的启用时间、保存位置及温度,复溶后的储存条件是否严格按要求执行,质控品若为液体质控,应考虑复温时间,复温时间过长或过短,都可能导致失控,甚至阳性质控不出;若为粉剂质控,还应考虑配制加样量是否准确,静置时间、混匀情况,很多初入PCR实验室人员可能因为紧张,出现加样不够准确,未及时混匀等情况。
除质控品原因外,还应考虑Taq酶、逆转录酶、核酸提取试剂是否失效,核酸试剂按照说明书要求存放,用前需复溶,复溶时间太长会导致酶活性降低甚至酶失活,试剂说明书中的保存条件不一定适用于已开盖试剂或开盖时间较长的试剂在临床实验室的使用,因此,复溶后应尽快将试剂使用完。若怀疑试剂导致的失控,需更换新试剂,重新检测。
应注意加样器与枪头是否匹配,核酸检测试剂加样量是否准确,阳性质控是否准确加入,加样过程是否避开交叉污染风险等。
若扩增仪孔间温度不一致,扩增孔位存在异物等可能会导致失控,应定期对扩增仪进行有效维护,必要时行背景荧光校正,早期发现可能存在的问题。
使用的离心管内存在扩增抑制物、操作中人员更换、实验室条件改变、试剂批号变更、核酸提取中靶核酸丢失、RNA降解等导致失控,需重新检测。
新冠核酸检测过程中遇到失控,首先观察质控样本和临床标本检测结果,根据检测结果分析失控原因,采取对应措施后重新检测质控标本和临床标本,确认失控问题是否解决,详细做好失控记录,定期回顾失控记录原因,加以持续改进,提高工作效率。
新冠核酸检测为新冠患者的确诊的重要依据,临床实验室应做好新冠核酸室内质控,定期关注室内质控的变化,及时发现可能存在的质控问题,以保证检测结果的准确可靠。
参考文献
[1].新型冠状病毒肺炎诊疗方案(试行第九版).
[2].李金明.实时荧光PCR技术[M].第二版.北京:科学出版社,2022.
[3].李金明,张瑞.新型冠状病毒感染临床检测技术[M].北京:科学出版社,2021.
[4].医疗机构新型冠状病毒核酸检测工作手册(试行第二版)
END